Якщо грати в асоціації, то слова «серце», «тиск», «гіпертензія» у більшості людей будуть пов’язані з поняттями «похилий вік», «пенсія», «пільги». І, мабуть, тільки одиниці згадають про підлітків, у яких, до речі, захворюваність на артеріальну гіпертензію (АГ) сягає 18%. Співвіднести дитячий вік і підвищення артеріального тиску складно навіть подумки. Не дивно, що у педіатрії ця проблема тільки починає вивчатися. Але й за наявними даними стає зрозумілим, що «навесні життя» сумнозвісне захворювання має багатогранний патогенез і дуже важко піддається лікуванню.
Якщо грати в асоціації, то слова «серце», «тиск», «гіпертензія» у більшості людей будуть пов’язані з поняттями «похилий вік», «пенсія», «пільги». І, мабуть, тільки одиниці згадають про підлітків, у яких, до речі, захворюваність на артеріальну гіпертензію (АГ) сягає 18%. Співвіднести дитячий вік і підвищення артеріального тиску складно навіть подумки. Не дивно, що у педіатрії ця проблема тільки починає вивчатися. Але й за наявними даними стає зрозумілим, що «навесні життя» сумнозвісне захворювання має багатогранний патогенез і дуже важко піддається лікуванню.
«Сонний» гормон
На відміну від літньої людини, яка уважно «прислухається» до будь-яких змін в організмі, підлітки майже ніколи не скаржаться на погане самопочуття. Власне, через це й немає точних статистичних даних щодо поширеності АГ у згаданої категорії пацієнтів. Зазвичай підвищений артеріальний тиск у них виявляється випадково, під час профілактичного огляду. І навіть після цього немає ніякої гарантії, що підліток пройде курс лікування. Оскільки АГ потребує тривалого прийому препаратів, нерідко від терапії відмовляються не тільки діти, а й навіть батьки. Тактика «навіщо дитину загодовувати таблетками» призводить до прогресування патології.
За таких обставин вкрай важливим стає розуміння механізмів формування АГ у пубертатному віці, що у перспективі дозволить ефективніше проводити відповідні профілактичні заходи.
На сьогодні основна роль у патогенезі АГ приділяється активації симпатичної нервової системи, що запускає цілий каскад змін у ренін-ангіотензин-альдостероновій системі. Але нещодавно стало відомо і про інші «пускові механізми», які сприяють розвитку патології у підлітків.
Зокрема, увагу вчених привернули ендокринні зміни, які відбуваються в організмі дитини після 10 років. Зараз активно вивчається взаємозв’язок АГ і порушення обміну мелатоніну — гормону епіфізу, основна функція якого полягає в регуляції циркадних ритмів. У дітей молодшого віку рівень цього гормону достатньо високий. Але з початком пубертату він різко знижується, і саме це запускає статеве дозрівання. На жаль, «падіння» рівня мелатоніну може чинити несприятливу дію на організм дитини, тому що вона стає схильною до порушення адаптативних процесів.
«Мелатонін дуже сильно корелює з рівнем кортизолу — основного гормону стрес-реалізуючої системи. І порушення співвідношення цих гормонів, на нашу думку, може суттєво впливати на перебіг АГ. З метою дослідити патогенетичну роль мелатоніну у формуванні первинної АГ у дітей і розробити лікувальні та профілактичні заходи, спрямовані на корекцію виявлених порушень, група авторів нашої кафедри провела дослідження за участю 109 дітей (52 дівчинки і 57 хлопчиків) віком від 10 до 17 років, у яких було виявлено підвищення артеріального тиску і виключено вторинний характер гіпертензії. Середній вік дівчаток склав 13,26±0,30 років, хлопчиків — 13,76±0,25 років», — розповідає Тетяна Гищак, кандидат медичних наук, доцент кафедри педіатрії №3 Національного медичного університету імені О.О. Богомольця.
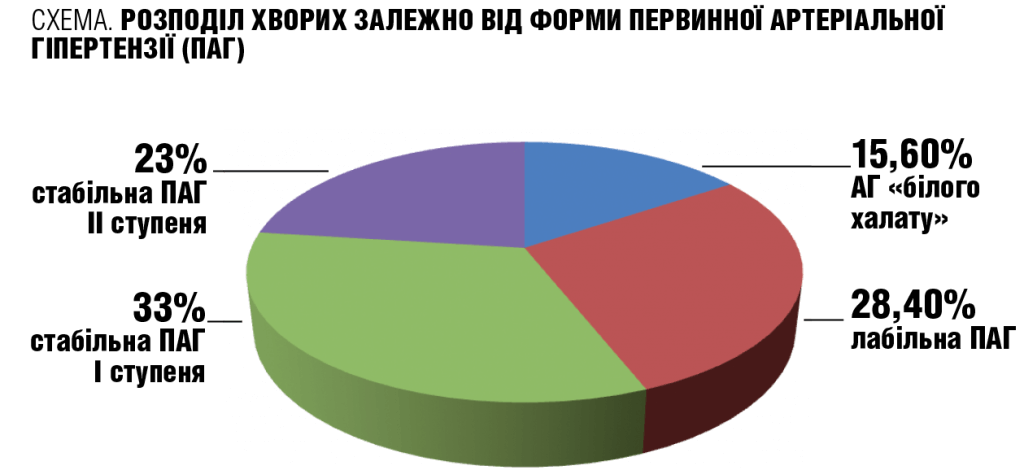
Переважну кількість хворих, що брали участь у дослідженні, склали діти зі стабільною АГ І ступеня, 23% хворих — з АГ ІІ ступеня, лабільна АГ спостерігалася у 28,4% підлітків. Також дослідники порівнювали дані з дітьми, які мали так звану АГ «білого халату», що являє собою межовий стан між нормою та АГ (див. схему).
«При дослідженні денної і нічної екскреції сульфат оксимелатоніну (6-СОМТ) із сечею у дітей з різними формами АГ ми з’ясували, що в контрольній групі був достатньо високий рівень нічної екскреції мелатоніну і низький — денної, що вважається нормальним, оскільки мелатонін повинен вироблятися під час сну. По мірі того, як відбувалося становлення гіпертензії у дітей, підвищувався і рівень денної екскреції мелатоніну, в той час як нічна екскреція мала хвилеподібну залежність. Зокрема, у дітей із лабільним перебігом зафіксовано найменшу різницю між денною і нічною екскрецією. А у дітей із стабільною АГ рівень нічної і денної екскреції гормону був найвищим, порівняно з іншими групами», — ділиться даними Т. Гищак. Тож, було зроблено висновок, що у дітей із первинною АГ спостерігається стресактивація мелатонін-продукуючої функції епіфізу. При відносно низькій продукції мелатоніну вночі формується лабільна АГ і кризовий її перебіг, у той час як при відносно високій нічній продукції відбувається стабілізація гіпертензії.
За словами спеціаліста, ненормальною «поведінкою» під час дослідження відрізнявся також рівень кортизолу. Виявилося, що найвищий він у дітей зі стабільною гіпертензією.
«Також ми вивчали рівень магнію в сироватці крові і сечі та отримали криву, подібну до рівня мелатоніну. Найменші показники магнію спостерігалися у дітей з лабільною гіпертензією. Ці діти клінічно характеризувалися кризовим перебігом захворювання, у них було найбільше скарг, спостерігалося різке коливання артеріального тиску, інколи навіть до втрати свідомості. І цей факт нас зацікавив, тому що саме в цій групі ми виявили найбільш виражені зміни», — підкреслює Т. Гищак.
Під час дослідження з’ясувалося, що денний мелатонін був пов’язаний з екскрецією кортизолу, а ось нічний його рівень мав схожу залежність із вмістом магнію в організмі. Найнижчими ці показники були в дітей із лабільною гіпертензією.
«Вивчаючи ступінь нічного зниження артеріального тиску, ми виявили, що у дітей саме із низьким його ступенем зафіксована найменша різниця між нічним і денним мелатоніном. Враховуючи залежність рівня мелатоніну від рівня магнію і зважаючи на досить високу кількість дітей з гіпомагніємією, ми включали у схеми лікування дітей препарати магнію», — розповідає Т. Гищак.
Активна тканина
Якщо «гормональний вибух» як чинник патології у підлітків можна певною мірою назвати закономірним, то участь судинного ендотелію у цьому процесі стала справжнім сюрпризом.
«Тривалий час ендотелій розглядався лише як пасивний бар’єр або фільтр. Сучасні дослідження доводять, що він є гормонально активною тканиною, яку сьогодні умовно називають найбільшою «ендокринною залозою» або «лабораторією», що безперервно виробляє величезну кількість біологічно активних речовин, які контролюють безліч важливих функцій», — розповідає Ірина Бессонова, кандидат медичних наук, асистент кафедри педіатрії Харківського національного університету ім. В.Н.Каразіна, співробітник ДУ «Інститут охорони здоров’я дітей і підлітків НАМН України».
Протягом останнього десятиріччя сформувався напрям, що розглядає судинний ендотелій як одну з патогенетичних ланок розвитку АГ і одночасно — як орган-мішень, що найраніше уражається при даному захворюванні.
Основними речовинами, які контролюють судинний тонус, є оксид азоту і ендотелін-1. У нормі їх вміст збалансований. Але при виникненні дисбалансу у співвідношенні вазодилататорів і вазоконстрикторів з переважанням останніх порушується вазорегулююча функція ендотелію з подальшим розвитком АГ. Одним із чинників, що сприяє розвитку ендотеліальної дисфункції, є підвищення рівня сечової кислоти у сироватці крові — гіперурикемія.
Експериментальні дослідження переконливо показали, що гіперурикемія сприяє розвитку АГ не тільки внаслідок її безпосереднього впливу на ендотелій судин, блокуючи виділення вазодилатуючих субстанцій і стимулюючи оксидативний стрес, але й через ураження тубуло-гломерулярного апарату нирок, зміну реальної гемодинаміки, безпосереднього індукування дисфункції гломерулярних ендотеліоцитів.
Гіперурикемія при АГ є однією з головних причин дисфункції ендотелію. Внаслідок неї блокується виділення оксиду азоту з ендотеліальних клітин, стимулюється оксидативний стрес з утворюванням вільних радикалів кисню, які є стійким чинником ураження ендотелію. Крім того, гіперурикемія активує протизапальні цитокіни, що є причиною ендотеліальної дисфункції.
Сечова кислота призводить до гіпертрофії мезангіальних клітин, експресії ними ангіотензину-2 та ендотеліну-1, сприяє гіпертрофії гладком’язових клітин внутрішньониркових артеріол і експресії нирковою тканиною реніну і ЦОГ-2», — пояснила І. Бессонова. За її словами, одним із ранніх проявів генералізованого ураження ендотелію з порушенням його проникності, у тому числі ендотелію клубочкового апарату нирок, є альбумінурія. Відображенням дисфункції ендотелію тубулярного апарату нирок служить підвищений рівень бета-2 мікроглобуліну в сироватці крові.
Оскільки розвиток захворювання у підлітковому віці залишається мало дослідженим, на базі ДУ «Інститут охорони здоров’я дітей і підлітків НАМН України» під керівництвом Миколи Коренєва, завідувача кафедри педіатрії, доктора медичних наук, професора, заслуженого діяча науки та техніки України, було проведено дослідження з метою виявлення ранніх ознак порушення ендотеліальної функції клубочкового і тубулярного апарату нирок у підлітків з АГ, з урахуванням рівня сечової кислоти в сироватці крові й індексу маси тіла пацієнтів.
«Ми провели дослідження серед 109 юнаків з АГ у віці 14-18 років. 29 із них (26,6%) мали нормальну масу тіла, 21 (19,3%) — надмірну, 59 (54,1%) страждали на ожиріння. Групу контролю склали 16 практично здорових однолітків. Під час дослідження визначався рівень сечової кислоти в сироватці крові, альбумінурії, бета-2 мікроглобуліну сироватки крові. Частота гіперурикемії у підлітків з АГ склала 56 %, нормоурикемія спостерігалася у 44 % учасників», — розповіла І. Бессонова.
Під час дослідження виявилося, що найчастіше юнаки, які мали одночасно АГ і гіперурикемію, страждали на ожиріння (56 % учасників).
При вивченні маркеру дисфункції ендотелію клубочкового апарата нирок — альбумінурії, встановлено, що її рівень у підлітків з АГ перевищував показники норми як у основній, так і в контрольній групі. У підлітків з гіперурикемією і нормальною масою тіла зареєстровано її найбільші значення, що перевищували аналогічні показники юнаків з гіперурикемією і надмірною вагою та ожирінням, а також усіх підлітків з гіперурикемією і різним рівнем підвищення маси тіла.
Взагалі альбумінурію виявлено у 48% досліджуваних, у тому числі у 52 — з гіперурикемією, у 42 — з нормоурикемією. У юнаків з ожирінням частота даного порушення значно збільшувалася за наявності супутньої гіперурикемії.
При дослідженні функціонального стану ендотелію тубулярного апарату нирок і його маркеру бета-2 мікроглобуліну сироватки крові було встановлено, що ці значення у підлітків з АГ взагалі не відрізнялися від аналогічних показників у контрольній групі, але достовірно зростали у підлітків з ожирінням і гіперурикемією. Частота ендотеліальної дисфункції тубулярного апарату нирок у підлітків з АГ складала 21%, при гіперурикемії — 23%, без неї — у 17%. У юнаків з ожирінням цей показник достовірно збільшувався при наявності гіперурикемії. Тобто, ендотеліальна функція клубочкового апарату нирок «страждала» значно частіше.
«Таким чином, ми бачимо, що дисфункція ендотелію гломерулярного і тубулярного апарату нирок у підлітків з АГ частіше спостерігається при поєднанні гіперурикемії з ожирінням. Підвищений рівень сечової кислоти в сироватці крові у хворих на АГ є «барометром» ендотеліальної дисфункції, у зв’язку з чим виявлення гіперурикемії з її подальшою адекватною корекцією дозволить покращити прогноз у хворих на АГ», — підсумувала результати дослідження І. Бессонова.
Винна генетика?
Окремий пул сучасних досліджень складає вивчення генетичних причин розвитку АГ у підлітків.
«Останніми роками відбувається пошук кандидатних генів і факторів ризику прогресування серцево-судинних ускладнень. Одним із таких генів-кандидатів визнаний ген ендотеліальної синтази оксиду азоту
3 типу, поліморфізм якого представлений алелем В та алелем А. В осіб у популяції з 5 алелями, які зустрічаються частіше, ніж із 4, спостерігається підвищений рівень нітратів у крові, який прямо пов’язаний зі швидкістю вироблення оксиду азоту. Залишається дискусійним питання генетичної схильності й ролі генотипу 4а4а у розвитку атеросклерозу, а також інших захворювань, що призводять до вироблення оксиду азоту», — відзначає Наталія Коновалова, кандидат медичних наук, асистент кафедри педіатрії №1 і неонатології Харківського національного медичного університету.
Генетична схильність до розвитку гіпертензії корелює з таким чинником, як порушення згортуваності крові. Зокрема, важливу роль тут відіграють циркулюючі в крові прокоагулянти. Відносно нещодавно до потенційних факторів ризику серцево-судинних ускладнень стали відносити і гіпергомоцистеїнемію.
Як відомо, гомоцистеїн — це природна сірковмісна амінокислота, яка не зустрічається в білках. Вчені відзначають, що у дітей із високим рівнем цієї амінокислоти в крові рано виникають важкі форми ураження артерій. Доведено, що гомоцистеїн може сприяти окисленню ліпопротеїдів низької щільності, порушенню функції ендотелію, проліферації гладком’язових клітин судин, а також активації тромбоцитів і коагуляційного каскаду. Тож виявлення гіпергомоцистеїнемії у підлітків з АГ може бути раннім маркером прогресування серцево-судинної патології.
До речі, у нормі рівень гомоцистеїну в плазмі крові у дорослих коливається в межах від 5 до 15 мкмоль/л; у дітей та підлітків середні значення цього показника складають 5 мкмоль/л.
 «Метою нашого дослідження було удосконалення ранньої діагностики ураження серцево-судинної системи у підлітків з артеріальною гіпертензією, гіпоталамічним синдромом пубертатного періоду шляхом вивчення поліморфізму гена ендотеліальної синтази оксиду азоту та рівня гомоцистеїну сироватки крові при різному генотипі. Для вирішення проблеми на базі Харківського обласного кардіологічного центру обстежено 113 підлітків у віці від 14 до 18 років. Критеріями включення були наявність епізодів підвищення артеріального тиску у дітей з надлишковою масою тіла. Групу контролю склали 12 здорових підлітків з нормальною масою тіла і артеріальним тиском», — розповіла Н. Коновалова.
«Метою нашого дослідження було удосконалення ранньої діагностики ураження серцево-судинної системи у підлітків з артеріальною гіпертензією, гіпоталамічним синдромом пубертатного періоду шляхом вивчення поліморфізму гена ендотеліальної синтази оксиду азоту та рівня гомоцистеїну сироватки крові при різному генотипі. Для вирішення проблеми на базі Харківського обласного кардіологічного центру обстежено 113 підлітків у віці від 14 до 18 років. Критеріями включення були наявність епізодів підвищення артеріального тиску у дітей з надлишковою масою тіла. Групу контролю склали 12 здорових підлітків з нормальною масою тіла і артеріальним тиском», — розповіла Н. Коновалова.
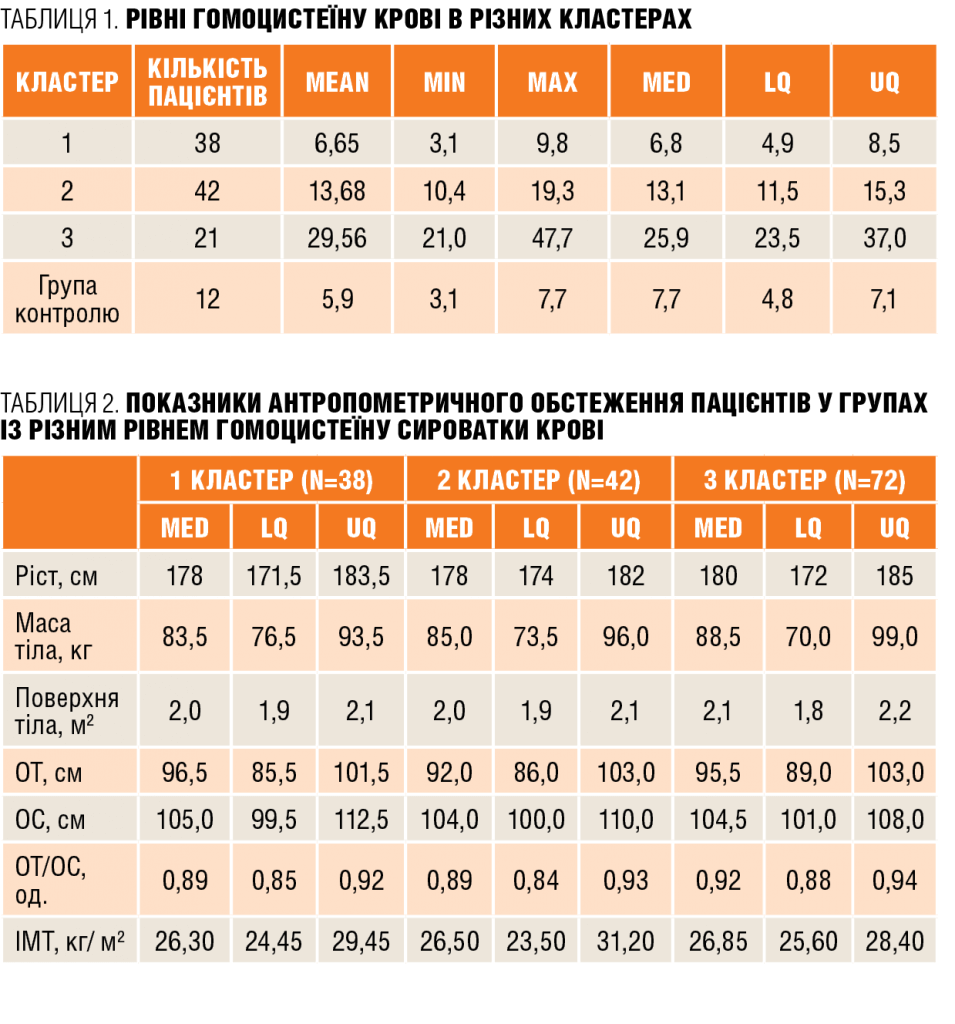
Спеціаліст звернула увагу на доцільність дослідження рівня гомоцистеїну методом кластерного аналізу, у результаті якого вдалося розподілити хворих на три кластери, які не пересікаються між собою (таблиця 1, 2).
«За результатами нашої роботи, звертає на себе увагу наявність абдомінального типу ожиріння у дітей з високим рівнем гомоцистеїну (група 3). При дослідженні показників артеріального тиску виявлено достовірні відмінності рівня середнього систолічного артеріального тиску протягом дня і ночі у пацієнтів з найвищим рівнем гомоцистеїну у сироватці крові. Достовірних відмінностей у росто-вагових показниках серед пацієнтів в різних кластерах не виявлено. Також ми з’ясували, що при нормальному рівні гомоцистеїну у сироватці крові модель геометрії лівого шлуночка залишалася у межах норми, по мірі прогресування рівня гомоцистеїну відзначався розвиток концентричного ремоделювання і концентричної гіпертрофії міокарда лівого шлуночка», — розповіла Н. Коновалова.
Що стосується генетичних відмінностей учасників дослідження, то генотип 4b4b був виявлений у 47 дітей, генотип 4b4а — у 43 дітей, генотип 4а4а — у 11. Серед них найнижчий вміст гомоцистеїну спостерігався у генотипу 4а4а.
«Згідно результатів дослідження, підвищення рівня гомоцистеїну сироватки крові у підлітків з АГ корелює з виразністю ремоделювання міокарда. Для пацієнтів з помірно підвищеним рівнем гомоцистеїну сироватки крові (13,68 ± 2,45 мкмоль/л) властиве концентричне ремоделювання лівого шлуночка. Для підлітків з найвищим його рівнем (29,56 ± 8,42 мкмоль/л) — за типом концентричної гіпертрофії міокарда лівого шлуночка, що відображає послідовність розвитку процесів ремоделювання міокарда. Відмінності рівня гомоцистеїну сироватки крові у пацієнтів з генотипом 4а4а, а також рівня тригліцеридів і ліпопротеїдів дуже низької щільності порівняно з показниками підлітків з генотипами 4b4b та 4b4а дозволяють віднести підлітків з генотипом 4а4а до групи підвищеного ризику за розвитком і прогресуванням АГ і пов’язаних з нею уражень органів-мішеней», — представила висновки досліджень
Н. Коновалова. Головною рекомендацією спеціаліста стало включення таких маркерів, як визначення рівня гомоцистеїну сироватки крові і поліморфізму гена ендотеліальної синтази оксиду азоту, в діагностику підлітків з АГ і ожирінням з метою прогнозування та своєчасної профілактики ускладнень серцево-судинної патології.
Звичайно, на тему АГ через її гостру актуальність написано вже тисячі наукових робіт. Але дослідження проблеми «з коріння», тобто з моменту формування патології, який нерідко припадає на підлітковий вік, на загальному тлі виглядають сиротливими. Проте навіть представлені поодинокі роботи підтверджують: поле для вивчення тут безмежне. І хоча в щоденній практиці лікар поки що не може застосовувати всі запропоновані методи діагностики, вони дають розуміння складності процесів, що передують появі у дитини АГ, — патології, яка залишається головною причиною інвалідизації та смертності у світі.
У статті використані матеріали науково-практичної конференції «Проблемні питання діагностики та лікування дітей з соматичною патологією».
Марина ЧІБІСОВА, «ВЗ»