З моменту, коли світ дізнався про появу нового вірусу SARS-CoV-2, пройшло трохи більше року. За цей час провели безпрецедентну кількість клінічних досліджень, вивчили структура вірусу, пояснили механізм формування імунної відповіді. Учені навіть змогли розробити вакцини проти небезпечного вірусу менш ніж за 12 місяців, що є видатним досягненням, враховуючи, що робота над такими препаратами зазвичай триває десятиліття або й більше.

Про все, що на сьогодні відомо про вакцини, які розроблені у світі проти вірусу SARS–CoV-2, а також рекомендації щодо щеплень і ймовірних алергічних реакцій у рамках освітнього проекту, організованого Національною медичною академією післядипломної освіти імені П.Л. Шупика розповідає Юрій Бісюк, доктор медичних наук, професор, експерт МОЗ України з питань дерматології, алергології, імунології, експерт комісії «Імуномодулятори та протиалергічні лікарські засоби» в ДП «Державний експертний центр МОЗ України».
Що наука сьогодні знає про патогенез вірусу SARS-CoV-2
 Юрій БІСЮК, доктор медичних наук, професор, експерт МОЗ України з питань дерматології, алергології, імунології, експерт комісії «Імуномодулятори та протиалергічні лікарські засоби» в ДП «Державний експертний центр МОЗ України»
Юрій БІСЮК, доктор медичних наук, професор, експерт МОЗ України з питань дерматології, алергології, імунології, експерт комісії «Імуномодулятори та протиалергічні лікарські засоби» в ДП «Державний експертний центр МОЗ України»SARS-CoV-2 – це РНК-вірус, який прикріплюється до клітин завдяки S-рецепторам (від англ. Spike – шип) на поверхні вірусу; він тропний до рецептора ангіотензинперетворюючого ферменту (АПФ). Саме АПФ є точкою входу для вірусу: субодиниці S-рецепторів активізуються і вірус проникає в альвеолярні клітини другого порядку, однак може атакувати і інші клітини організму людини. Усередині соматичної ядровмісної клітини вірус починає розмножуватися, синтезуючи свою РНК. Одночасно проходять два процеси: реплікація зі створенням РНК і транскрипція з новоутворених ділянок для синтезу субодиниць М, N, E і S (S – spike, E – envelope, М – membrane, N – nucleocapsid). Потім вірус за допомогою клітинних структур ендоплазматичного ретикулума (ЕПР) і апарату Гольджі збирає вірусні частинки, які у вигляді зрілих віріонів виходять з клітини і інфікують інші клітини.
Однак із вірусом взаємодіють також і дендритні клітини – це особлива популяція клітин імунної системи, які можуть захоплювати вірусні частинки і представляти їх на своїй поверхні у вигляді МНС для Т-клітин. Потім починається класична імунна відповідь, коли вірусні білки діляться на маленькі пептиди (епітопи), які приєднуються до спеціальних рецепторів МНС другого типу або рецепторів головного комплексу гістосумісності. Тобто дендритна клітина є ніби посередником між вродженою і набутою імунною відповіддю. Така клітина направляється у найближчий лімфатичний вузол, де взаємодіє з наївним Т-хелпером. Останній, у свою чергу, стимулює В-лімфоцити до синтезу імуноглобуліну G, а також Т-хелпери першого типу і цитотоксичні Т-лімфоцити. Отже, імунна відповідь завжди закінчується утворенням імуноглобулінів проти вірусних частинок і утворенням специфічних високоактивних СD8-клітин або цитотоксичних Т-лімфоцитів.
З одного боку, імуноглобуліни будуть зв’язувати білки і віруси, наприклад, вони можуть зв’язати S-рецептори вірусу, з іншого боку, цитотоксичні Т-лімфоцити можуть знайти заражену вірусом клітину і за допомогою механізмів апоптозу запустити процес її загибелі. Тож імунна відповідь має дві основні складові: утворення антитіл і утворення цитотоксичних Т-лімфоцитів.
Зараз увага лікарів часто зосереджена на антитілах до вірусу SARS-CoV-2. Можна почути глобальні висновки про те, що наявність високого рівня антитіл – це хороша ознака, і, навпаки, якщо антитіл мало, то це погано. Однак, крім цього важливого фактора, необхідно також пам’ятати про утворення клітин пам’яті: Т- і В-лімфоцитів. При контакті з вірусом імунна система формує імуноглобуліни G, M, а після клінічного одужання концентрація цих антитіл падає. Але залишаються клітини пам’яті Т- і В-лімфоцити, особливість яких полягає в тому, що при повторному попаданні вірусу ці клітини відразу активізуються. В-лімфоцитам уже не потрібно 7-14 днів, щоб почати синтезувати специфічні імуноглобуліни G, вони роблять це миттєво.
Про особливості створення вакцин
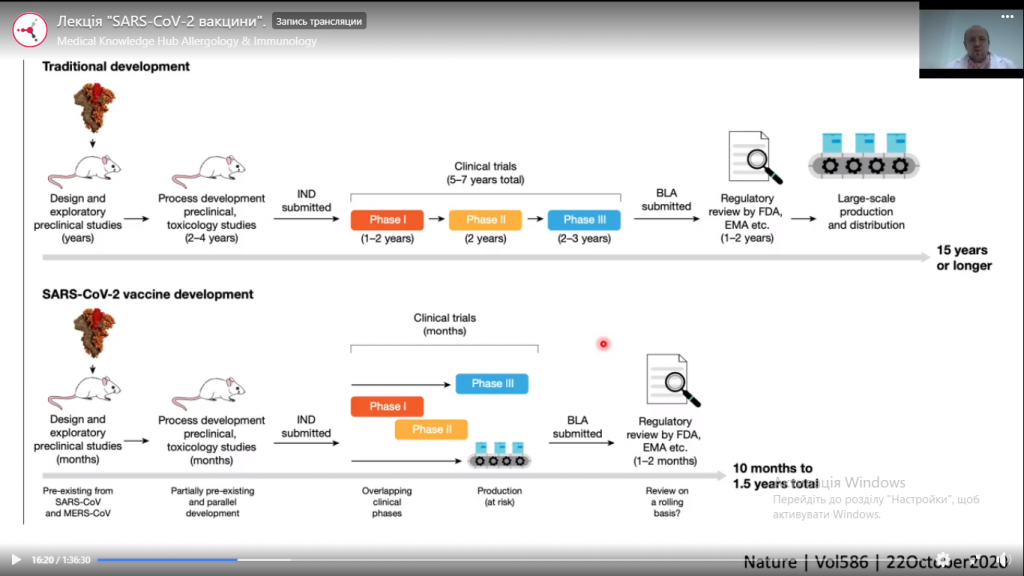
Як уже зазначалося, розробка нових вакцин триває десять і більше років. І те, що сьогодні у світі є препарати, дія яких захищає проти небезпечного вірусу SARS-CoV-2, і які були створені менш ніж за 12 місяців, є видатним досягненням сучасної науки.
Зазвичай доклінічні токсикологічні дослідження на лабораторних тваринах тривають в середньому 2-4 роки. Після вивчення імуногенності на тваринах, токсикологічних особливостей і здатності зв’язувати певні рецептори переходять до фази клінічних досліджень. Перша фаза проводиться на здорових добровольцях, на другій визначають імуногенність різних доз. На третій фазі до досліджень залучають велику кількість пацієнтів (15-17 тисяч), які беруть участь у випробуваннях протягом 5-7 років. Загальний час, який вчені зазвичай витрачають на створення вакцини становить 10-15 років.
Специфіка вакцин для COVID-19 полягає в тому, що вони були розроблені в середньому за 10 місяців. При цьому першу і другу фазу клінічних досліджень об’єднали, а на третій фазі вже були отримані попередні результати – тобто третя фаза почалася, коли друга ще не завершилася.
За даними ВООЗ, станом на 3 лютого 2021 року в розробці знаходиться 289 експериментальних вакцин проти SARS-CoV-2. З них 66 перебувають на різних етапах клінічних випробувань, 20 – на третій фазі дослідження.
За даними Lancet тільки п’ять із цих 66 вакцин, розроблені AstraZeneca, Pfizer, Gamaleya, Moderna і Sinopharm, були схвалені відповідними регуляторними органами.
Ще п’ять вакцин – з Китаю, Індії, Казахстану і Росії – отримали схвалення або дозвіл на використання в надзвичайних ситуаціях іншими регуляторними органами. Деякі з організацій, що розробляють ці вакцини, надали ВООЗ документацію для включення своїх препаратів у список для використання у надзвичайних ситуаціях. Але ці документи все ще розглядаються.
Також очікується, що незабаром вакцини від Novavax і Johnson & Johnson буде дозволено використовувати на підставі позитивних проміжних результатів третьої фази досліджень.
У цьому контексті варто зазначити, що регуляторні органи типу FDA (Управління з санітарного нагляду за якістю харчових продуктів і медикаментів) і EMA (Європейське агентство лікарських засобів) зазвичай рік або два тільки розглядають матеріали клінічних досліджень, адже це 10-20 томів. Сьогодні ці організації вивчають документи 1-2 місяці. Не стала винятком у цьому питанні і Україна. Наразі у нас дозволена реєстрація вакцин протягом 5 днів, з урахуванням вихідних.
Сім видів вакцин проти одного вірусу
Вірус SARS-CoV-2 належить до сімейства коронавірусів. Його особливість полягає у тому, що для прикріплення до клітини він використовує S-рецептори, котрі зв’язуються з рецепторами ангіотензинперетворюючого ферменту (АПФ). Сьогодні структура цих рецепторів досить добре вивчена. S-рецептор – це тример, що складається з трьох субодиниць, кожна з яких ділиться на S1 і S2. Субодиниця S1 містить спеціальні домени, амінокислотні ділянки яких називаються receptor-binding domain, і саме вони зв’язуються з рецептором ангіотензинперетворюючого ферменту. Такі ділянки мають сувору послідовність амінокислот, яка ідеально підходить до АПФ. Ці послідовності надзвичайно цікавлять вчених, оскільки саме цю ділянку і потрібно заблокувати за допомогою імуноглобуліну G. Тобто потрібна вакцина, яка створить імуноглобуліни класу G, а вони вже зв’яжуть receptor-binding domain.
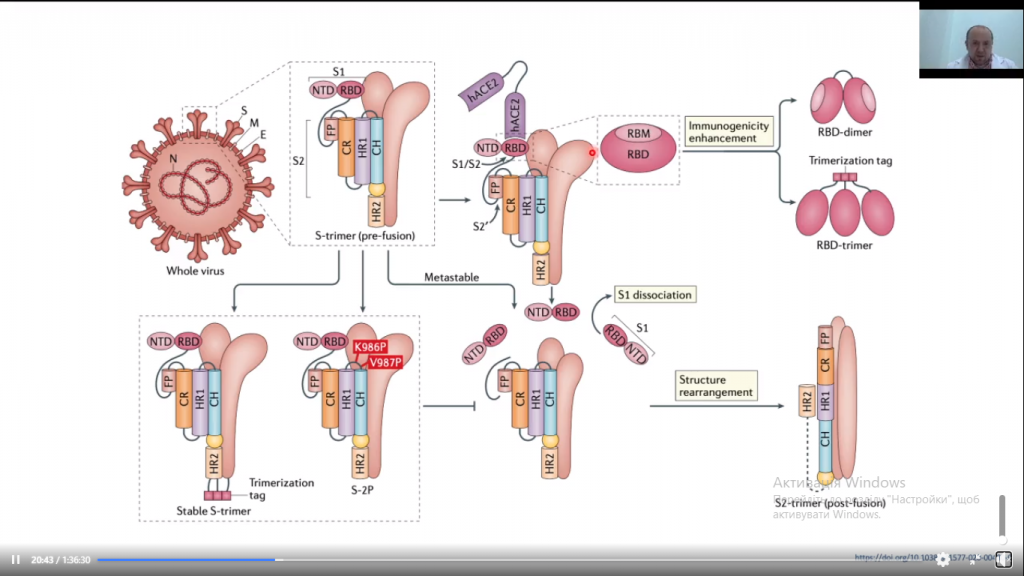
На сьогодні існує 7 видів вакцин (деякі з них перебувають у розробці) проти SARS-CoV-2:
- Живі ослаблені вакцини. Розроблені методом генної інженерії і містять модифікований вірус, який не може спровокувати захворювання.
- Інактивовані вакцини. Виробляються за старою технологією: обробкою формальдегідом або при нагріванні, внаслідок цих процесів відбувається інактивація будь-якої патогенної ділянки. Основний недолік цього виду вакцин полягає у тому, що для утворення імунної відповіді необхідна велика кількість клітин, тому ослаблені вакцини в цьому сенсі більш перспективні.
- Вірусно-векторні вакцини. У аденовірус впроваджується частка гена, що кодує частину гена S-білка, який потім вводиться людині. Сам аденовірус не є патогенним, однак тут вступають у дію дендритні клітини, які захоплюють цей вірус і процесують його. В результаті утворюється іммуноголобулін класу G до спайкового білку вірусу. Ці вакцини можуть провокувати сильну імунну відповідь. Спочатку їх використовували для створення вакцини проти вірусу Ебола.
- ДНК-вакцини. Доставляються у клітину за допомогою методу електропорації. При потраплянні ДНК всередину ядра з неї утворюється інформаційна РНК, яка стимулює трансляцію білків S-рецепторів, які процесуються дендритними клітинами. Імунна відповідь у подальшому схожа на ту, котра виникає під час дії вакцин, які описані вище. На сьогодні поки не існує ліцензованих ДНК-вакцин.
- РНК-вакцини. Вважаються надзвичайно безпечними, оскільки це не сам вірус, а тільки частина його генів. Вони можуть відразу ж почати трансляцію білків S-рецепторів. Наразі ліцензовані дві вакцини такого виду від Pfizer і Moderna.
- Субодиничні білкові вакцини. Синтезовані білки S-рецепторів зв’язуються з N-протеїном. В результаті утворюється певна структура, що є дуже імуногенною.
- Вірусоподібні частки. По суті, це порожня оболонка вірусу, що не має генома вірусу; на її поверхні знаходяться білки S-рецепторів, які і викликають імунну відповідь.
Що відомо про безпеку вакцин
Наразі найбільш дослідженими вважаються субодиничні білкові вакцини, а також РНК-вакцини від Pfizer і Moderna. Щодо останніх, то ніхто не вірив у їхню ефективність, однак попри скепсис, який супроводжував процес їх розробки на початкових стадіях, вони створені. Більше того, деякі з них вже успішно і масово застосовуються у багатьох країнах світу.
Вакцини, вже схвалені регуляторними органами або знаходяться на третій, завершальній фазі.
- Вакцини Pfizer і BioNTech BNT162b2 – схвалена
Це РНК-вакцини, які помістили у особливі ліпідні бульбашки (lipid delivery vehicle). Після внутрішньом’язової ін’єкції ці бульбашки потрапляють у клітини, де починається реплікація. Отримані антигени потрапляють в дендритні клітини і починається класична імунна відповідь: виробляються імуноглобуліни G до S-рецепторів вірусу.
На третій фазі було скриновано 44 тис. пацієнтів; серед яких 18 556 отримали вакцину Pfizer, а 18 530 отримали плацебо. Це велика вибірка, яка дає більше даних для роботи і більш точні середні значення, необхідні для проведення статистичного аналізу. Серед учасників було трохи більше чоловіків, ніж жінок; 82% склали представники європеоїдної раси, 9,2% – негроїдної. Ці дані добре екстраполюються і на українську популяцію. Вік добровольців: 18-55 років – 57%, більше 55 років – 42%.
Побічна дія. В основному учасники скаржилися на біль у місці введення. У групі 16-55 років після першої дози важкі побічні ефекти виникали менш, ніж у 1%; побічні реакції середньої тяжкості спостерігалися у 30%. Також у незначної кількості пацієнтів були помітні почервоніння і набряк. Підвищення температури до 38-38,4° С протягом кількох днів зафіксовано у всіх вікових групах як після першого введення, так і після другої дози. Зрідка спостерігалася слабкість, головний і м’язовий біль, озноб, болі в суглобах. В середньому у 20-40% людей, які отримали вакцину, мали побічні реакції. Такі ж показники фіксують при застосуванні будь-яких інших вакцин, у тому числі, і вакцин проти сезонного грипу.
Ефективність. За допомогою статистичних інструментів було підраховано, що ефективність вакцини становить 90,3-97,6%. Незважаючи на вакцинацію, деякі учасники захворіли; з них 5 пацієнтів з групи 16-55 років, 3 пацієнта понад 55 років і 1 пацієнт з групи понад 65 років. Для групи старше 75 років ефективність склала 100%. Для європейців ефективність показала 95%, для афроамериканців – 100%.
- Вакцина mRNA-1273, Moderna – схвалена
Відрізняється високою імуногенністю і викликає хорошу імунну відповідь, що дає підстави заявляти про перспективність цієї вакцини.
На третій фазі було рандомізовано 30 тис. учасників. З них 14 тис. –контрольна група (отримали плацебо), а 14 тис. – експериментальна.
Побічна дія. Досить часто виникав незначний біль у місці введення – 75%, біль середньої тяжкості – 10%. Почервоніння практично не виникало. Зрідка спостерігалася набряклість у місці введення. У невеликої кількості учасників – легкий ступінь лімфоденопатії. У значної кількості учасників зафіксовано підвищення температури, слабкість, біль у м’язах, артралгії, озноб.
Ефективність. 89,3-96,8%, в середньому – 94,1%. У групі пацієнтів старше 55 років – 95%, понад 65 років – 86,4%. У порівнянні з Pfizer, ефективність цієї вакцини у групі літніх людей є нижчою. Ризик виникнення тяжкого перебігу захворювання – 4 випадки з експериментальної групи і 44 випадки з контрольної групи.
Важливо підкреслити, що вакцини Pfizer, BioNTech і Moderna необхідно вводити протягом 5 днів після виходу з умов наднизьких температур (-70° C). Крім того, не існує м-РНК вакцин, які були б схвалені раніше.
- Вакцина Covid-19 Vaccine ChAdOx1-S recombinant, AstraZeneca – схвалена
У геномодифікований аденовірус шимпанзе був введений генетичний матеріал вірусу SARS-CoV-2. Сам аденовірус не є патогенним для людини. Після введення вакцини починається звичайна імунна відповідь, яка призводить до утворення імуноглобулінів класу G і інших класів, а також до активації Т-клітин.
При дослідженні безпеки були використані різні режими введення цих вакцин. Проводячи скринінг своїх препаратів, Pfizer і Moderna пішли класичним шляхом і ділили учасників на 2 групи: контрольну (плацебо) і експериментальну. Щодо вакцини від AstraZeneca, тут був застосований сучасний аналіз з великою кількістю груп і підгруп.
В результаті було встановлено, що у всіх вікових групах сформувалася практично однакова концентрація антитіл. Також вивчалася здатність виділяти гамма-інтерферон, який є фактором, котрий виділяють Т-хелпери першого типу, що стимулюють клітинний імунітет. Ця вакцина має високу імуногенність у всіх групах після бустерної дози.
Побічна дія: артралгія, міалгія, почервоніння, симптоми, які виникають при грипі і грипоподібних станах.
Ефективність: 70,4% з довірчим інтервалом 54,8-80,6%. Наразі дослідження щодо ефективності тривають.
- NVX CoV2373 для мутантних форм вірусу, Novavax – третя фаза дослідження
Це спайковий білок, з’єднаний з Matrix-M – ад’ювантом, який підсилює імунну відповідь. Використання ад’ювантів є перспективним напрямком для розробки вакцин і проведення іммуноспецифічної аллергентерапіі.
Механізм дії цієї вакцини можна описати так: ДНК кодує інформацію спайкового білка, з ДНК утворюється матрична РНК, яка є інструментом для трансляції білків і спайкового білка.
Також вивчалася імунна відповідь від Т-хелперів першого типу, який на 28-й день показав їх активацію, а значить Т-хелпери вбиватимуть заражені вірусом клітини.
У третю фазу досліджень було включено 15 тис. добровольців. Ефективність склала 89,3%, довірчий інтервал – 75,2-95%.
За допомогою ПЛР-діагностики було доведено, що ця вакцина ефективна проти оригінального вірусу SARS-CoV-2 в 95,6% випадків і в 85,6% – проти мутованого британського штаму. Поки це дані опубліковані на сайті виробника, проте вже зараз можна сказати, що вакцина є досить перспективною. Її введення призводить до утворення великої кількості антитіл навіть у порівнянні з тими, хто перехворів SARS-CoV-2 у важкій формі.
- Вакцина Sinovac – третя фаза дослідження
Наразі про цю вакцину відомо найменше. За інформацією видання Lancet Sinovac і його партнери, які брали участь у дослідженні, повідомили про різний рівень ефективності вакцини. Дані базуються на основі третьої фази досліджень. Зокрема у Бразилії (50%), Індонезії (65%), Туреччини (91%) та Об’єднаних Арабських Еміратах (86%). Вакцина виготовлена на основі інактивованого вірусу. Проміжні результати третьої фази не публікувалися в рецензованих журналах; дані були взяті з прес-релізів компаній або дослідників, які проводять клінічні випробування.
Вакцини проти SARS-CoV-2: алергічні реакції і протипоказання
Наразі усі авторитетні світові організації дотичні до охорони здоров’я наголошують, на тому, що алергічні захворювання та наявність алергії на лікарські препарати і харчові продукти не є протипоказанням для проведення вакцинації проти SARS-CoV-2. Перед щепленням медичним працівникам необхідно зібрати анамнез у пацієнтів, щоб передбачити і вжити запобіжних заходів щодо ймовірних негативних реакцій. Наприклад, рекомендувати зробити аналіз на триптазу.
Рекомендації Європейської академії алергії та клінічної імунології (EAACI) щодо попередження виникнення алергічних реакцій при вакцинації SARS-CoV-2.
- Якщо у пацієнта спостерігалася гіперреакція на перше введення, його необхідно направити у спеціалізований алергологічний центр для обстеження. Алерголог проводить пацієнтові шкірний прик-тест до компонентів вакцини (рекомендується базофільно-провокаційний тест з використанням необхідних протоколів). Після отримання усіх результатів необхідно надати рекомендації щодо проведення подальшої вакцинації.
- Після щеплення медичним працівникам рекомендується 15 хвилин спостерігати за станом пацієнта, а людям не покидати місця проведення вакцинації, перебуваючи у спеціально відведених для цього зонах (в українських рекомендаціях час спостереження за пацієнтом після проведення вакцинації – 30 хвилин).
- Якщо у анамнезі виявлено неконтрольований перебіг бронхіальної астми або були випадки анафілаксії, такі пацієнти повинні провести більше часу під наглядом медиків. Однак протипоказань до проведення вакцинації у них немає.
- При виникненні генералізованої кропив’янки (є передвісником анафілактичного шоку), генералізованого свербежу (pruritus), появі задишки, свистячого дихання, набряку язика пацієнту необхідно негайно у зовнішню частину стегна ввести внутрішньом’язово епінефрин 0,3 мг в автоінжекторі (або звичайний адреналін 0,5 мг).
- У разі анафілактичного шоку кожні 15 хвилин вводиться адреналін. При бронхоспазмі – сальбутамол інгаляційно. При відсутності позитивного ефекту необхідно викликати бригаду швидкої допомоги і транспортувати пацієнта у реанімаційне відділення.
Важкі алергічні реакції можуть виникнути у будь-якої людини, незалежно від наявності у неї алергії до будь-чого. Найближчим часом кількість різного виду вакцин буде збільшуватися, а відтак з’явиться можливість підібрати найбільш підходящий варіант для імунізації.
Як довго зберігається імунітет проти SARS-CoV-2
Висновки і висловлювання експертів щодо цього питання наразі дуже обережні, адже напрацювання даних ще триває. Зокрема, американські фахівці з Центру контролю і профілактики захворювань США (CDC), кажуть про те, що у перші 90 днів після перенесеної інфекції SARS-CoV-2 реінфекція не є частою.
Експерти також не дають чітких прогнозів щодо того, який відсоток людей потрібно вакцинувати для формування колективного імунітету. Спеціалісти CDC зазначають, що наразі будь-яка інформація стосовно цього питання буде некоректною.
Якщо пацієнт вже перехворів на SARS-CoV-2, це не є підставою відмовлятися від вакцинації, оскільки після хвороби не завжди виробляється стійкий імунітет і відомі важкі випадки перебігу недуги при повторному інфікуванні. Однак, якщо при лікуванні SARS-CoV-2 використовувалися моноклональні антитіла або реконвалесцентна плазма, необхідно почекати 90 днів і тільки потім пройти процедуру щеплення.
Фахівці переконують: проводити одночасно вакцинацію проти грипу та SARS-CoV-2 можна. Між цими щепленнями необхідно зробити інтервал 14 днів.
Щодо вакцинації вагітних, наразі компанії Pfizer та BioNTech лише оголосили, що запрошують жінок, які перебувають при надії, отримати щеплення проти коронавірусу для проведення клінічних досліджень препарату.
CDC рекомендує вагітним жінкам від 45 років і старшим, у яких діагностовано ожиріння або цукровий діабет, провести вакцинацію проти SARS-CoV-2.












вірус змінюється (мутація) … і як ті вакцини діють щодо нових штамів вірусу???