Сьогодні медичні фахівці та виробники ліків ніяк не можуть позбутися відчуття захвату з приводу ефективності нових імуноонкологічних засобів — моноклональних антитіл. Успіх цих препаратів, шалені темпи їх розробки та численні дослідження дещо відвертають увагу від інших можливостей імунотерапії раку, а саме потенціалу ДНК-вакцин.
ДНК-вакцини належать до класу принципово нових біологічних препаратів. З їх розробкою пов’язують великі надії на підвищення ефективності профілактики не тільки хвороб бактеріальної чи вірусної природи, а й онкологічних захворювань. Основні компоненти ДНК-вакцини — вектор і цільовий імуноген. Тобто в класичному варіанті такі препарати складаються з плазмідних ДНК, що містять гени збудників інфекцій або мутантних клітин. Продукти цих генів здатні спричиняти захисні реакції організму, виконуючи в цьому випадку роль антигенів.
Різними шляхами потрапляючи в організм, синтетична ДНК «просочується» в ядро клітини, «монтується» в геном, перетворюючи клітину на «фабрику» з виробництва вакцини — стимулює її до продукування білків, що опосередковують формування імунної відповіді.
ДНК-вакцини: проста конструкція та складні методи доставки
Фактично цей підхід можна визначити як персоналізовану імунотерапію раку, продукти якої виготовляють у кілька етапів. Спочатку виявляють характерні мутації: зі зразка пухлини пацієнта секвенують послідовності, котрі потім порівнюють із генетичними послідовностями нормальних клітин. Для націлювання обирають одну чи кілька мутантних послідовностей, й на основі цього виготовляють вектор або плазміду, які згодом мають кодувати антигени. Потім отриману композицію вводять пацієнту.
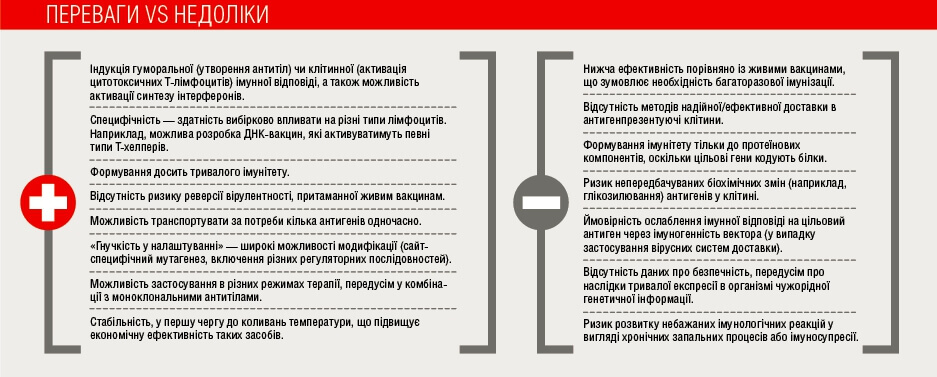
 Втім, незважаючи на простоту конструкції, багато механізмів розвитку імунної відповіді на ДНК-вакцини не до кінця вивчені. Пластичність дизайну ДНК-вакцини — головна перевага таких засобів: їх компоненти можна міняти й комбінувати залежно від цілей численними методами генної інженерії. Конструкція може включати один або кілька антигенів, геникостимулятори, різні регуляторні елементи тощо, а також кодувати білки, котрі визначають транспорт і метаболізм заданого антигену.
Втім, незважаючи на простоту конструкції, багато механізмів розвитку імунної відповіді на ДНК-вакцини не до кінця вивчені. Пластичність дизайну ДНК-вакцини — головна перевага таких засобів: їх компоненти можна міняти й комбінувати залежно від цілей численними методами генної інженерії. Конструкція може включати один або кілька антигенів, геникостимулятори, різні регуляторні елементи тощо, а також кодувати білки, котрі визначають транспорт і метаболізм заданого антигену.
Проте ця проста конструкція вимагає складних методів доставки. До сьогодні розроблено багато різних підходів для отримання специфічних антинеопластичних відповідей на введення ДНК-вакцини проти раку.
Річ у тім, що істотним недоліком ДНК-вакцин є низька імуногенність. Проблему намагаються вирішити, змінивши спосіб доставки — препарати вводять методом електропорації. У цій методиці фізичної доставки генів використовують електричний імпульс для генерування перехідних пор у клітинній плазматичній мембрані, що дає змогу ефективно переносити ДНК у клітини. Формування пори відбувається дуже швидко — приблизно за 10 наносекунд.
Електропорація допомогла значною мірою подолати такі проблеми, як низький рівень трансфекції і недостатня імуногенність. Численні досліди на тваринах й останні клінічні дослідження показали, що ДНК-вакцини, котрі доставляють методом електропорації, здатні обумовити стійкіші специфічні імунні реакції й зменшити тяжкість захворювання. Цей метод з успіхом застосовували в кількох клінічних випробуваннях, зокрема у пацієнтів з раком передміхурової залози, лейкемією, колоректальним раком, меланомою тощо.
Розробка ДНК-вакцин від раку: сучасний стан
На сьогодні в розробці біотехнологічних компаній та університетів перебувають близько півтисячі ДНК-вакцин проти захворювань різної етіології, й певна частина з них належить до онковакцин. Щодо деяких протиракових вакцин проводять клінічні випробування останніх фаз і, можливо, незабаром їх буде впроваджено в клінічну практику. Зокрема, на пізніх стадіях клінічних досліджень перебувають вакцини проти раку шийки матки, голови і шиї, мозку тощо.
Американська компанія, що спеціалізується на розробці ДНК-вакцин, створила препарат проти дисплазії шийки матки VGX-3100, який наразі проходить третю фазу випробувань. Кілька років тому на Всесвітньому конгресі з вакцинації VGX-3100 отримала нагороду «Краща терапевтична вакцина». Ця компанія також підтримує розробку аналогічних проектів, спрямованих на профілактику гліобластоми та деяких інших видів раку.
Вказаному методу боротьби з онкологічними захворюваннями велику увагу приділяють й інші організації. Наприклад, ефективність продемонструвала ДНК-вакцина проти лейкемії, створена в Саутгемптонському університеті (Велика Британія), — її вводять за допомогою електропоратора. Засіб спрямований на інгібування гена WT1 (білка пухлини Вілмса-1), підвищену активність якого визначають у злоякісних клітинах різних типів.
На жаль, для клінічного застосування схвалено лише одну подібну вакцину — Sipuleucel T (Dendreon Corporation), яку застосовують при раку передміхурової залози. Фахівці пояснюють нетипово повільні темпи прогресу в цій галузі передусім тим, що протиракові вакцини дозволяють випробовувати на пацієнтах з останніми стадіями захворювання, коли активація чи посилення природної імунної відповіді вже не забезпечує вираженого ефекту. Але все ж таки прогрес є, й деякі вчені вважають, що протягом найближчих 15 років онкологи поповнять свій арсенал ще одним надійним типом зброї, котрий допоможе їм подолати рак.

Не лише рак
Хоча сьогодні такий підхід ще видається технологією майбутнього, насправді ідея використовувати гени збудників захворювань для активації захисних механізмів виникла понад 20 років тому. Упродовж цього періоду ДНК-вакцини пройшли певну еволюцію, передусім, відзначається прогрес у дизайні нуклеотидних послідовностей і оптимізації складу (у тому числі включення молекулярних ад’ювантів), а також в удосконаленні форм і методів доставки.
Наразі сконструйовані численні експериментальні ДНК-вакцини для профілактики інфекційних захворювань паразитарної (шистосомоз, лейшманіоз), бактеріальної (хламідіоз, сибірка, мікоплазмоз) і вірусної (сказ, лихоманка Ебола) природи. На різних стадіях доклінічних і клінічних випробувань перебувають ДНК-вакцини проти вірусів грипу, гепатитів А і В, герпесу, тропічних геморагічних лихоманок, ВІЛ тощо.
Любомира Протасюк, спеціально для «ВЗ»











