Найважливіший інгредієнт у складі будь-якого препарату — активна речовина, вона і є власне сам препарат. Решту складників, котрі відомі нам під загальною назвою «допоміжні речовини», використовують для стабілізації — мало хто цікавиться їх окремими назвами. Але тепер ці «невідомі» відіграють усе важливіші ролі у всій формулі, оскільки від них очікують особливої роботи — значного підвищення ефективності лікарського засобу.
Зелена хімія популярного напою
Журнал Biomaterials повідомив, що американські дослідники створили інноваційний гель для доставки лікарських речовин, у якому в ролі каталізатора використовується кофеїн. (Мода на зелену органіку не оминула навіть такі «суворі» синтетичні наукові галузі, як біотехнологія та біоінженерія.)
Кофеїн — широко відома речовина, котра славиться здатністю допомагати нам залишатися бадьорими. Однак, здається, команда дослідників з Масачусетського технологічного інституту та жіночої лікарні Брігама придумала для цього стимулятора нове застосування, яке, напевне, змінить імідж кофеїну назавжди. У попередніх дослідах продемонстровано, що в процесі утворення полімерних матеріалів кофеїн здатен виконувати роль ефективного каталізатора, тобто може діяти як слабка основа. Це відкриття дало змогу вченим розробити новий метод створення біосумісних липких гелів, котрі можна застосовувати в ролі транспортних систем для доставки ліків (а теоретично — використовувати й з іншими медичними цілями).
Утім, поки що автори зосередилися на транспортних системах доставки ліків. Отримані експериментаторами складні поліефіри містять невелику кількість кофеїну — приблизно стільки, скільки у середньостатистичній чашці чаю. У попередніх тестах на безпечність небажаних побічних ефектів дослідники не виявили. За словами вчених, головна цінність кофеїну — його натуральність.
Під час синтезу полімерних гелів використовують безліч хімічно активних каталізаторів, але їх недолік у тому, що вони пошкоджують під час контакту чутливі речовини. Наприклад, таке часто трапляється при спробах вдосконалення транспорту біологічних препаратів.
У наш час для виготовлення полімерних гелів зазвичай потрібні каталізатори-метали, які можуть бути небезпечні, коли залишаться в осаді після повного циклу утворення матеріалу. Учені з Масачусетського технологічного інституту за допомогою кофеїну змогли повністю знешкодити носій — гель залишається безпечним навіть у разі ковтання. У своїй останній роботі дослідники продемонстрували на тваринній моделі та in vitro, що вони можуть «заповнювати» такі транспортні гелі двома протималярійними препаратами, після чого лікарські засоби (артесунат і піперахін) залишаються ефективними та контрольованими.
Автори очікують, що новий матеріал також використовуватиметься для транспорту інших класів ліків, передусім призначених для перорального застосування, оскільки це найзручніший і найпоширеніший спосіб уведення. Дослідники стверджують: препарати на основі цього гелю можна також випускати у формах для розжовування для пацієнтів, які зазнають труднощів з ковтанням капсул і таблеток, а також дітей.
Важливо, що розробникам досить просто контролювати такі властивості носія, як міцність, структура поверхні та швидкість вивільнення активних інгредієнтів, тобто міняти хімічні та механічні властивості гелю. Це досягається завдяки елементарній корекції його складу. Наприклад, вони вже отримали таким шляхом «кофеїнові» поліефіри, котрі містили або поліетиленгліколь, або інший полімер, поліпропіленгліколь. Так само вчені створили «кофеїновий гель», який об’єднував ці два найпопулярніші фармакологічні полімери у різних співвідношеннях.
Зміна властивостей поверхні матеріалу може допомогти дослідникам контролювати швидкість проходження гелю через травний тракт. «Залежно від завдань і активних речовин, виробник зможе створити оптимальну для себе суміш. Наша мета полягала в тому, аби спростити метод виготовлення та зберегти покращений профіль безпечності поліефіру, використовуючи потенційно безпечніші каталізатори, — і нам це вдалося», — запевняють розробники.
Стрімкий прогрес з перспективами на майбутнє
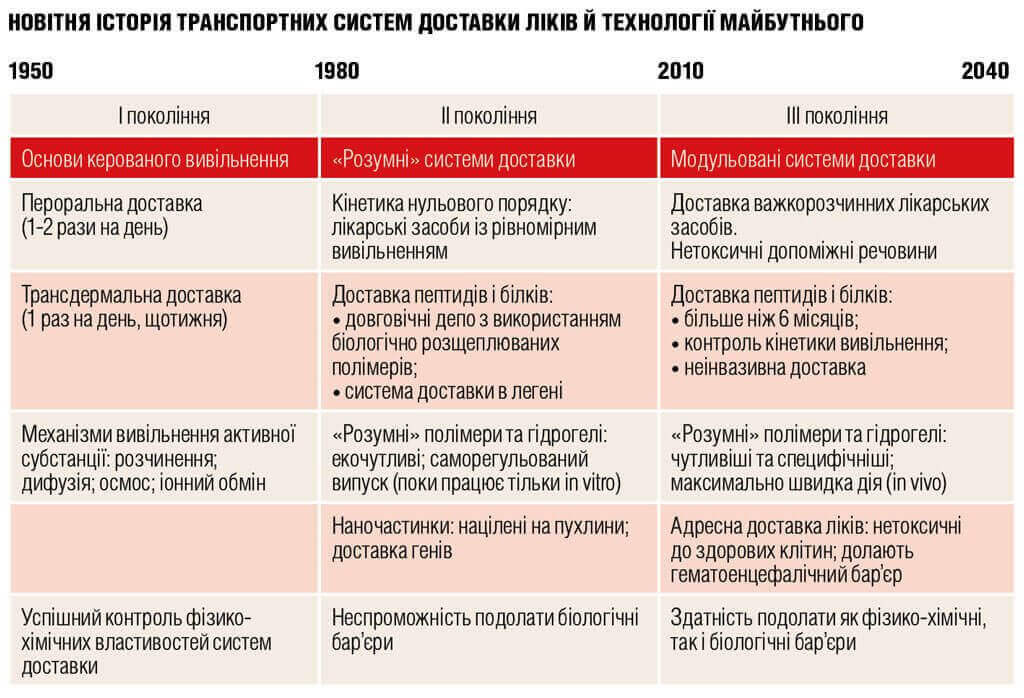
Насправді історія розробки технологій контрольованої доставки ліків розпочалася не так давно: в 1952 році одночасно з винайденням першої формули тривалого вивільнення. До 1950 року активна речовина всіх засобів, котрі випускалися в таблетках або капсулах, вивільнялася одразу після контакту з водою. У 1952 році Сміт Клейн Бічем «сконструював» першу композицію зі стійким уповільненим вивільненням, яка давала змогу контролювати кінетику вивільнення препарату та досягти 12-годинної ефективності. Технологія, котра нині відома, як «спансула» (капсула для внутрішнього застосування, що містить суміш мікродраже з різним часом розчинення), дала можливість задавати швидкість дії медикаментозної терапії.
Нові комбінації, котрі виникали за нею, називали різними термінами («стійкий випуск», «сповільнений випуск», «пролонгована дія»), але фактично вони мало відрізнялися між собою. І завданням І покоління таких транспортних систем була розробка оральних та трансдермальних форм з тривалим вивільненням та встановлення контрольованих механізмів вивільнення лікарських речовин: вказаний період обмежується 50-80-ми роками минулого століття. За цей час наука отримала більшість фундаментальних уявлень про механізми вивільнення лікарських засобів, особливо в пероральних і трансдермальних формах (див. таблицю), що пришвидшило розробку багатьох таких форм, серед яких найпоширенішими виявилися розчинні та дифузні препарати. Осмотичні композиції були нечисленними й популярними недовгий час. Так само не прижився в медицині й іонообмінний механізм.
Препарати ІІ покоління (1980-2010 роки), на відміну від І, не стали так само успішними (якщо вимірювати успіх кількістю зареєстрованих засобів), й частково це пояснюється неймовірною складністю формул та завдань, які ставили перед собою розробники. Також їх було важко втілити в клінічну практику, наприклад, саморегульовані системи доставки інсуліну працюють досить добре в лабораторних умовах, але втрачають ефективність in vivo. Пізніше біотехнологи зосередилися на вивченні композицій із наночастинок, особливо — на випробуваннях їх профілю безпечності.
Підготувала Любомира ПРОТАСЮК, спеціально для «ВЗ»