Перш ніж революційні технології успішно інтегруються в ту чи іншу галузь медицини, їм доводиться пройти через безліч зльотів і падінь. Нові платформи лікування раку не є винятком із цього правила. Який саме етап зараз переживає онколітична віротерапія, вирішували онкологи на третьому щорічному саміті, що відбувся 5-7 грудня у Майямі.

Онколітична віротерапія — новітня методика, що полягає у застосуванні реплікаційно-компетентних вірусних векторів для знищення ракових пухлин. Метод лікування злоякісних пухлин онколітичними вірусами, котрі руйнують злоякісне новоутворення, — наймолодша галузь клінічної онкології, що здобуває дедалі більше визнання серед фахівців. Проте, незважаючи на юний вік, метод уже встиг побувати і в репутаційних скандалах. Утім, не будемо забігати так далеко, спочатку — тільки гарні новини.
Вірус як… препарат
Онколітичні віруси — терапевтично корисні протиракові віруси, які селективно інфікують і ушкоджують злоякісні новоутворення, не завдаючи шкоди нормальній тканині.
Кожному вірусові властивий специфічний клітинний тропізм, що допомагає визначити, які тканини в першу чергу атакує збудник. Усім відомо, що рабівірус ушкоджує нейрони, вірус гепатиту В — гепатоцити, ВІЛ — Т-лімфоцити, вірус грипу — епітелій дихальних шляхів тощо. Багато, якщо не більшість, вірусів виявляють тропізм до пухлин і пухлинних клітин, хоча й не ексклюзивний. Це явище пов’язано, швидше, з біологією пухлин, аніж з біологією вірусів.
 Очевидно, що основною умовою успіху онколітичної вірусотерапії є специфічне таргетування злоякісних клітин, тобто вибіркова активність. Деякі віруси, такі, як парвовіруси, реовіруси, вірус Ньюкасла, природно віддають перевагу раковим клітинам, натомість аденовірус чи вірус простого герпесу можуть бути адаптовані або модифіковані з тим, щоб зробити їх специфічними для злоякісних клітин.
Очевидно, що основною умовою успіху онколітичної вірусотерапії є специфічне таргетування злоякісних клітин, тобто вибіркова активність. Деякі віруси, такі, як парвовіруси, реовіруси, вірус Ньюкасла, природно віддають перевагу раковим клітинам, натомість аденовірус чи вірус простого герпесу можуть бути адаптовані або модифіковані з тим, щоб зробити їх специфічними для злоякісних клітин.
Наразі найнадійніший спосіб «націлювання» вірусів на злоякісні клітини — це селективне усунення небажаних тропізмів шляхом інженерних маніпуляцій із генетичним апаратом патогену. Таким чином життєвий цикл вірусу вдається селективно заблокувати у відповідній (здоровій) тканині-мішені.
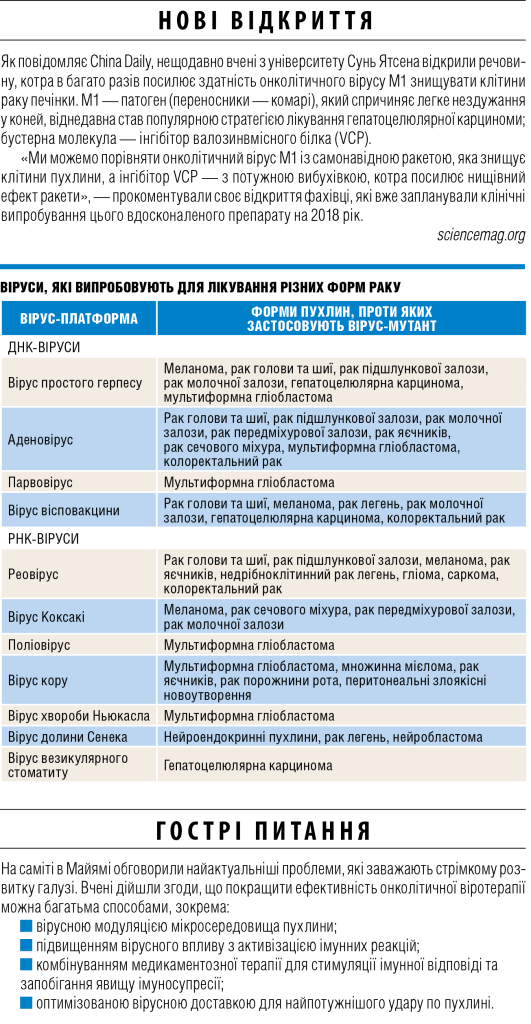
Різні моделі поведінки вірусу-мутанту
Онколітичні віруси можуть знищувати інфіковані злоякісні клітини по-різному, починаючи від явища прямої вірусної цитотоксичності, тобто лізису, й закінчуючи низкою цитотоксичних імуноефекторних механізмів. За допомогою звичайних моделей загибелі клітин (апоптоз, некроз або аутофагія) описати складні сценарії вбивства ракових клітин під час віротерапії належним чином фактично неможливо.
Терапевтичний ефект віротерапії обумовлений тим, що онколітичний вірус, як і належить такому патогену, підкорює та контролює весь механізм запрограмованої загибелі інфікованої клітини. І, не зважаючи на те що вона ракова, тобто «безсмертна», вірус урешті-решт її вбиває, оскільки безжально експлуатує наявні клітинні ресурси для синтезу та збору нових вірусних часток. Простіше кажучи, околітичний вірус до смерті виснажує живучу злоякісну клітину.
Рецепторів, які можуть відкрити модифікованим вірусам «ворота» для вторгнення в ракову клітину, теж чимало. Це і поверхневі рецептори EGFR, і HER2/neu, і рецептор фолієвої кислоти, і нектини тощо.
Окрім безпосереднього вбивства інфікованих клітин онколітичні віруси можуть також слугувати посередниками у знищенні неінфікованих ракових клітин за допомогою непрямих механізмів: шляхом руйнування пухлинних кровоносних судин, посилення специфічних протипухлинних імунних реакцій тощо.
Піонери галузі
Незважаючи на геніальну простоту фармакокінетики цих природних «ліків» й широке коло можливостей генної інженерії, піонери галузі — американці та китайці — почали випробовувати метод на добровольцях відносно недавно, трохи більше ніж 10 років тому.
У листопаді 2005 року Shanghai Sunway Biotech (м. Шанхай, Китай) оголосила про схвалення регуляторами Китаю аденовірусного мутанта H101 для лікування раку носоглотки у поєднанні з хіміотерапією на основі цисплатину.
Схвалення китайських регуляторів ґрунтувалося на результатах рандомізованого контрольованого дослідження, у якому порівнювали ефективність H101 і стандартної хіміотерапії цисплатином та 5-фторурацилом, а також застосовували його у поєднанні зі стандартною терапією. Вірусний препарат вводили безпосередньо в пухлини голови та шиї.
Проте це не було першою спробою: до такого способу використання онколітичного вірусу група Onyx Pharmaceuticals вдалася в 1999 році під час проспективного контрольованого дослідження, у якому ефективність препарату Onyx-015 у поєднанні з хіміотерапією перевіряли на вибірці пацієнтів з раком голови та шиї. Уражені вірусом пухлини демонстрували значно більшу частоту відповіді та триваліший час до прогресії, ніж контрольні пухлини. На жаль, це дослідження передчасно згорнули. Ні, не через небажані явища чи побічні ефекти, а… внаслідок корпоративного поглинення компанії-ліцензіата.
 Таким чином, США віддали першість на цьому полі Китаю. На щастя, китайці довели дослідження до переможного кінця: його результати підтвердили терапевтичні властивості онколітичного аденовірусу. Виявилося, що комбінація внутрішньопухлинного введення H101 та хіміотерапії давала 79% терапевтичної відповіді порівняно із 39,6% у разі проведення лише хіміотерапії.
Таким чином, США віддали першість на цьому полі Китаю. На щастя, китайці довели дослідження до переможного кінця: його результати підтвердили терапевтичні властивості онколітичного аденовірусу. Виявилося, що комбінація внутрішньопухлинного введення H101 та хіміотерапії давала 79% терапевтичної відповіді порівняно із 39,6% у разі проведення лише хіміотерапії.
Хоча ці результати й відкрили багато перспектив, на вчених чекало безліч перешкод. Серед перших — питання доставки. Незважаючи на те що для деяких типів і стадій пухлин (наприклад, локалізований рак голови та шиї) може бути корисною місцева нехірургічна терапія (зокрема, системну регресію пухлини спостерігали після ін’єкції безпосередньо в меланоми), переважна більшість онкопацієнтів все ж потребує системної терапії.
Сумнівно, що H101 або його «кузен» Онікс-015 коли-небудь набули б широкого застосування при метастатичних новоутвореннях — хоча б тому, що можливості їх доставки надто обмежені (внутрішньовенна доставка аденовірусів до пухлин дуже неефективна). До того ж маніпуляції з геномами вірусів знижували онколітичний потенціал препаратів на їх основі.
Експериментально-доказова медицина
Препарати для внутрішньовенного введення почали випробовувати на інших збудниках. З новими вірусотерапевтичними агентами перспективи галузі виглядають дещо оптимістичніше: їх системне застосування стало можливим завдяки оптимізованій доставці вірусу до пухлин. Це досягається кількома шляхами, наприклад, через точний вибір типів вірусів, які найкраще проникають у пухлини через кров.
Таким чином, незабаром було доведено, що внутрішньовенна терапія вірусами Ньюкасла спричиняє об’єктивні реакції у хворих на колоректальний рак і гліобластому. Сьогодні випробовують абсолютно різні способи введення таких препаратів:
- інтратуморальний — безпосередньо в пухлину (найпоширеніший);
- внутрішньовенний;
- пероральний;
- внутрішньом’язовий;
- ректальний;
- інгаляційний;
- у мозок (convection-enhanced delivery).
Окрім цього, ученим вдалося підвищити потенціал онколітичної віротерапії в інший спосіб — шляхом індукції цитотоксичних Т-лімфоцитів, тропних до пухлини.
Утім, на цьому фронті дослідники поки що зазнають більше поразок, аніж перемог: фактично терапевтична ефективність препаратів часто виявляється не такою вираженою, як очікувалося на підставі доклінічних випробувань. Численні вірусні препарати зазвичай не доходять до третьої фази клінічних досліджень.
Але й тут є приємні винятки. Першою віхою, що знаменувала успіх клінічної онколітичної віротерапії, стало завершення III фази дослідження ефективності препарату на основі вірусу простого герпесу T-VEC, або талімогену лагерпарепвеку (talimogene laherparepvec), у лікуванні метастатичної меланоми. T-VEC — перший онколітичний вірус, затверджений FDA у жовтні 2015 року.
Виклики, що чекають на цю галузь, — відбір «переможців» серед онколітичних платформ та різноманітних похідних, кількість яких постійно збільшується, що забезпечить оптимальні терапевтичні результати.
Плями на вірусах
 Виявляється, тінь можна навести навіть на репутацію найзловісніших патогенів. Якщо задати в пошук «онколітична віротерапія» російською, можна знайти безліч, м’яко кажучи, сумнівних сторінок, на яких розповідається про надзвичайну ефективність препарату Rigvir. Навіть лікарю зовсім неважко сприйняти його за панацею, а що вже казати про пацієнтів та їх рідних, які перебувають у відчаї?
Виявляється, тінь можна навести навіть на репутацію найзловісніших патогенів. Якщо задати в пошук «онколітична віротерапія» російською, можна знайти безліч, м’яко кажучи, сумнівних сторінок, на яких розповідається про надзвичайну ефективність препарату Rigvir. Навіть лікарю зовсім неважко сприйняти його за панацею, а що вже казати про пацієнтів та їх рідних, які перебувають у відчаї?
У 2016 році латвійські ЗМІ розповіли, що Ейнар Репше, колишній прем’єр-міністр і екс-президент Банку Латвії, оголосив про своє рішення очолити «Фонд віротерапії Айни Муценіеце». Колишній політик викликав суцільне здивування, коли зголосився керувати «однією з ланок складної та вкрай сумнівної маркетингової мережі холдингу Rigvir».
Незважаючи на те що препарат не пройшов і третини належних випробувань, 2004 року він був зареєстрований латвійським Державним агентством ліків, а з 2011 року Rigvir внесли до переліку засобів, які компенсуються пацієнтами з діагнозом «меланома (рак шкіри)». У 2015 році Національна служба охорони здоров’я затвердила клінічне керівництво з лікування раку шкіри, згідно з яким Rigvir визнано допустимою ад’ювантною терапією після хірургічного втручання.
У базі наукових досліджень знайшлося кілька робіт з випробування цього препарату. Цікаво, але в 90-ті роки минулого століття його називали «вірусний імуномодулятор», пізніше — «препарат для імунотерапії», й лише за останні кілька років він «виріс» до «засобу для онколітичної терапії». Й справді, за трендами потрібно стежити.
Високі сподівання
«Це ще не кінець. Це навіть не початок кінця. Але це, мабуть, уже кінець початку», — так сказав Вінстон Черчілль, коли дізнався про першу перемогу британських військових у Другій світовій війні. Приблизно те саме говорять нам перші клінічно значущі результати, які нещодавно було отримано на ниві онколітичної віротерапії.
На жаль, науковці — теж люди, яким властиво розчаровуватися в найперспективніших інноваціях, коли ті не дадуть «належних» результатів. Що ж, початкове збудження, котре виникає після перших вдалих експериментів, часто викликає безпідставний оптимізм. Це заважає долати подальші перешкоди і вже може досить швидко перетворитися на безпідставний песимізм.
Подібної долі зазнала, наприклад, терапія моноклональними антитілами, яку спочатку вітали оплесками як потенційну «магічну кулю», що допоможе вбити рак. Проте згодом, після ранніх клінічних невдач, її вже вважали приреченою на забуття. Та, на щастя, вірні послідовники проігнорували цей необґрунтований песимізм й невтомно працювали, незважаючи на всі перешкоди — щоб нарешті дати тисячам пацієнтів ефективні моноклональні антитіла. І вже сьогодні ніхто не заперечуватиме, що такі агенти, як ритуксимаб, трастузумаб чи цетуксимаб, зробили революцію в клінічній онкології.
Онколітична вірусна терапія — нехай інша за принципом дії, але фактично та сама за інноваційністю терапевтична стратегія, котру ще потрібно ретельно перевірити в безлічі випробувань. Але вже сьогодні не викликає сумнівів те, що вона пройде цей шлях і врешті-решт досягне успіху.
Любомира Протасюк, спеціально для «ВЗ», за матеріалами molecular-therapy.com, rus.delfi.lv, stm.sciencemag.org











